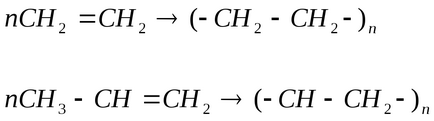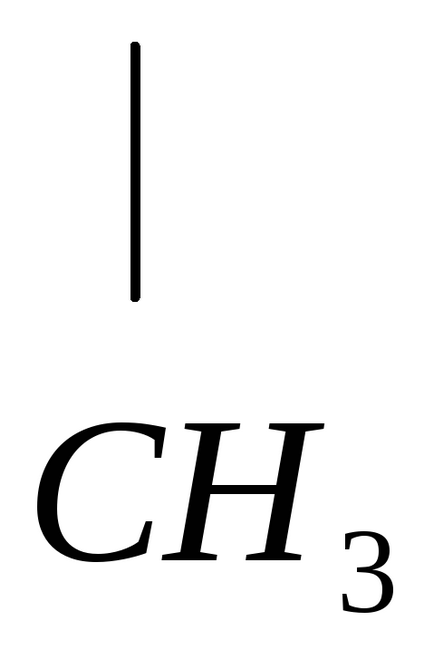етилен въглеводороди
Двойната връзка в молекулата на етилен - комбинация от един и -он комуникация. Приблизително енергия -връзка 350 кДж / мол, комуникация 262.4 кДж / мол. Дължината на връзката между въглеродните атоми е 0.134 пМ.
2.2. Химичните свойства на алкени
химични свойства, определени от присъствието на олефини в тяхната молекула -връзка. Да бъдеш по-energodostupnoy, -връзка е прекъсната и освободените валентност въглеродните атоми са похарчени за присъединяване на атоми или групи от атоми. Йонни присъединяват реагенти за -връзката е електофилния характер Ade (от думата добавянето на английски - и се присъединяват към Латинска електрофилно - електрофилно любящ отрицателни).
Под влияние на електронен облак -олефин халоген молекула е поляризирана, като по този начин образува индуциран дипол.
Положителен край на дипол действа като електрофилен реагент и улавя -електрони на двойната връзка за образуване на нестабилен комплекс:

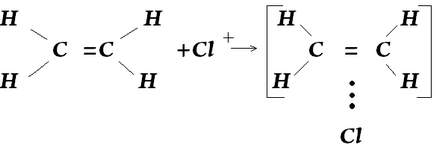
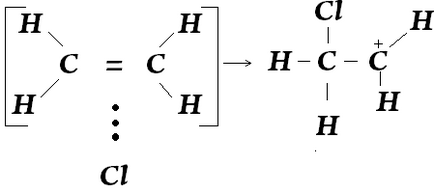
В етап II -връзка и връзка хлоро-хлоро heterolytically счупен. Хлоро поради етилен -електрони образува конвенционален -връзка с един от въглеродните атоми. Този въглероден атом движи да посочи SP 3 атомна орбитална хибридизация. Вторият въглероден атом на двойната връзка, като загубили електрони, положително заредена, и сместа се превръща в carbocation частици (на частиците с положителен заряд върху въглен). Положително заредени въглероден атом, към карбокатиони е в SP 2 хибридизация. Carbocation наричан -сложна.
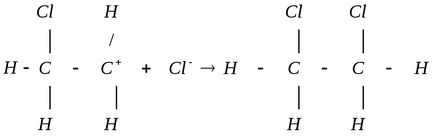
В етап III процес carbocation чрез взаимодействие с аниона на Cl -. форми с това -връзка поради електронна двойка анион.
Реакцията на свързване може да бъде:
1) хидрогениране (добавяне на водород) протича в присъствието на Pt катализатори. Pd или Ni:
2) Халогениране (присъединяване Cl2 Br2) .:
Присъединяването Br2 на олефин - отговор качество за откриване на етилен въглеводороди. На преминаване етилен през разтвор на Br2 във вода като жълто-кафяв разтвор обезцветяване възниква в резултат на реакцията на добавяне.
3) Gidrogalogenizirovanie (присъединяване халид)
VV Markovnikov изучаване реакцията на добавяне на халогеноводороди на алкени асиметрични, създадена следния модел: водород се прибавя на мястото на двойната връзка на най-хидрогенира (свързан с голям брой водородни атоми) е въглероден атом, халоген - до най хидрогенира. От гледна точка на електрон теория Markovnikov правило може да се обясни както следва: в резултат на два етапа електрофилно допълнение към два различни стабилност carbocation може да бъде оформен като междинни съединения:
От тях първата е най-стабилен. Следователно, електрофилно допълнение към двойната връзка са в посока на образуване на най-стабилната carbocation междинно съединение I:

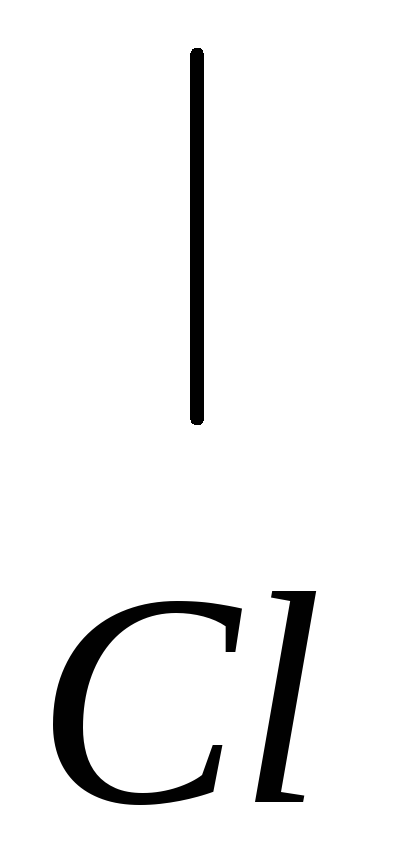
4) Хидратация (присъединяване вода)
В присъствието на катализатор (с концентрирана H 2SO 4. ZnCl2) е прикрепен към алкени вода до образуване алкохоли. Реакцията протича в съответствие с член Markovnikov.
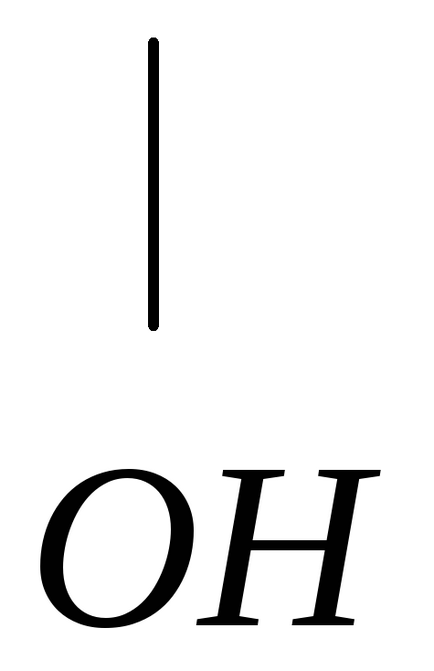
Реакцията на полимеризация се оставя да се получи високо молекулно съединение - полиетилен и полипропилен